Вы, возможно, слышали, что все тела состоят из молекул, эти молекулы хаотически движутся и взаимодействуют. Чтобы применять эти положения в физике, нужно описать молекулы как самостоятельные физические тела. Нужно выяснить, какие размеры они имеют, какую массу, с какой силой взаимодействуют, с какими скоростями движутся. Выяснить, сколько их, в конце концов…
Проще всего, конечно, заглянуть в справочники, но гораздо интереснее самому «на пальцах» получить основные физические характеристики молекул – размеры, массу и т.д.
Оказывается, это можно сделать с помощью простейших рассуждений и опытов на собственной кухне. А потом можно и в справочники…
1. Размер молекулы
Характерный (типичный) размер молекул можно оценить, поместив каплю масла на поверхность воды. Капля начнет расплываться до тех пор, пока ее молекулы не расположатся в один слой. Тогда толщина этого слоя – это и есть примерный размер молекулы. Измерить толщину этого слоя напрямую трудно, зато можно его вычислить, считая пятно цилиндром.

Тогда, очевидно, размер
![]()
где
 – объем капли, R – радиус пятна.
– объем капли, R – радиус пятна. Автор этой идеи, великий физик Рэлей, получил в результате измерений

современные точные измерения дают такой же порядок величины.
Проявляется ли как-то размер молекул в привычных для нас масштабах?
Пример 9
В плену у крокодилов
Во время Второй мировой войны наши лётчики перегоняли гидросамолёты. Экипаж одного гидроплана, пленённый красотой африканского озера, совершил посадку в незапланированном месте. Самолёт удачно приводнился, и тут лётчики заметили, что озеро кишит крокодилами.
“Взлетаем!” – решили лётчики, но прямо по курсу – крокодил… А кто гарантирует, что рядом не всплывёт ещё один?
Трагизм положения в том, что стоит одному из поплавков гидроплана попасть в животное – и аварии не избежать. Подстрелить крокодила? Но тогда “сбегутся” его кровожадные сородичи, и будет ещё хуже… Как быть?
Летчики плеснули на воду кружку бензина. Когда бензиновое пятно дошло до крокодилов, они очистили «взлетную полосу», и летчики смогли взлететь.
Очевидно, радиус бензинового пятна на поверхности напрямую связан с размером молекулы бензина. Оценим радиус пятна:
Весь бензин из стакана(рис) превратился в пятно толщиной

Объем пятна VП, с одной стороны, равен объему бензина в стакане VБ. С другой стороны, этот объем
VП,=Sh=πR2∙ a0
(мы для упрощения предположили, что пятно имеет форму «блина», т.е. цилиндра с радиусом основания R и малой высотой a0).
Приравнивая эти объемы, получим
VБ = πR2∙ a0,
откуда
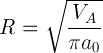
Если объем кружки VБ = 0,5 литра=5∙10-4м3, получаем R ≈ 1250 м.
2. Масса молекулы
Теперь можно оценить характерную массу молекулы. Если считать, что в твердом теле и жидкости молекулы упакованы плотно, касаясь друг друга, то можно считать, что плотность вещества близка к плотности молекул. Тогда масса молекулы:

Например, для молекулы воды имеем
 кг,
кг,Можно ли определить массу молекулы точнее?
Из химии известно, что масса любой молекулы с неплохой точностью выражается как целое число «атомных единиц» – масс водородного атома. Точная величина атомной единицы массы
 кг
кгТогда точное значение массы любой молекулы находим, зная химический состав молекулы и беря атомные массы из таблицы Менделеева. Например, для молекулы воды получим
 кг
кг3. Число молекул
Зная массу молекулы, легко подсчитать число молекул в заданной массе вещества m, если вещество состоит из молекул одного сорта.
Поскольку в веществе нет ничего, кроме молекул, очевидно, число молекул
 (1),
(1),соответственно

Например, в килограмме воды число молекул
Теперь можно определить концентрацию молекул (число в единице объема):
 (2),
(2),Заодно получим линейную концентрацию nl (число молекул на единицу длины) и поверхностную концентрацию ns (число молекул на единицу поверхности).
Для этого рассмотрим кубик вещества, состоящего из плотно упакованных молекул (рис.2). Выразим ребро этого кубика, площадь грани и объем через размер молекулы:



Отсюда, зная число молекул в объеме кубика, легко получить число молекул вдоль ребра кубика
 (3),
(3),и число молекул на грани кубика
 (4),
(4),Если принять ребро рассмотренного кубика за единицу длины, получим аналогичные соотношения для концентраций:
 (5),
(5), (6),
(6),
